RAK(RetroNectin Active Killer)免疫疗法是过继免疫治疗的重要分支,其核心原理是从患者外周血中采集免疫细胞(主要为 CD8⁺T 细胞与 NKT 细胞) ,在体外通过白细胞介素 - 2(IL-2)、干扰素 -γ(IFN-γ)等细胞因子激活,经 RetroNectin 技术扩增至 10⁹-10¹⁰量级后回输体内,形成具有强杀伤活性的 “免疫军团”。
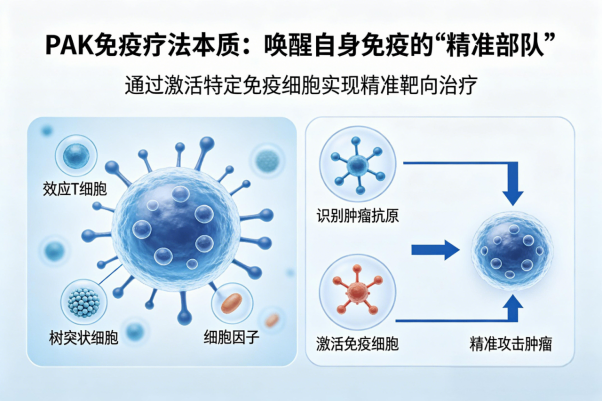
与传统治疗不同,RAK 细胞通过三重机制发挥作用。
1、直接杀伤:表达 NKG2D 等受体,精准识别肿瘤细胞配体并裂解
2、免疫调节:分泌 TNF-α、IFN-γ 等细胞因子,激活巨噬细胞、NK 细胞等协同作战
3、微环境重塑:减少肿瘤组织中免疫抑制细胞,维持 DC 细胞与细胞毒性 T 细胞的抗原呈递功能。
实体瘤治疗的关键证据
1. 肝癌术后防复发:改写 70% 复发魔咒
中国医学科学院肿瘤医院与北京医院联合开展的 II 期临床试验显示,对肝癌根治术后高危患者(肿瘤直径大、微血管侵犯等),每季度输注 RAK 细胞(3 个周期,1×10¹⁰细胞 / 次),1 年无复发生存率达 79%,3 年达 68% ,较对照组(中位无复发生存期 13.2 个月)风险比降至 0.31(P=0.017)。长期随访(最长 63 个月)未发现严重不良反应,仅轻微注射部位反应与短暂疲劳。
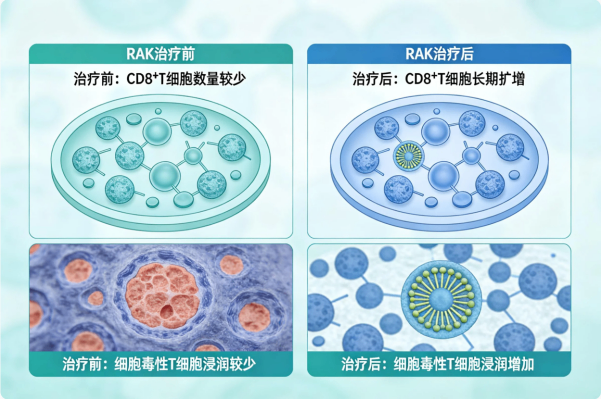
机制研究证实,RAK 治疗可使患者体内 CD8⁺T 细胞长期扩增,肿瘤组织中细胞毒性 T 细胞浸润增加,即使复发也能抑制免疫微环境恶化。
2. 转移性肾癌:三线治疗新选择
针对既往治疗失败的转移性肾癌(mRCC)患者,I 期剂量递增试验(ChiCTR1900021334)显示,RAK 细胞输注后33.3% 患者肿瘤缩小,2 例实现持续部分缓解。治疗后患者外周血 CD3⁺、CD8⁺T 细胞计数显著升高,IL-2 与 IFN-γ 峰值水平与疗效正相关,且无细胞因子释放综合征(CRS)等严重毒性。
3. 胃癌攻坚:脐带血 RAK 开启新赛道
解放军总医院正在开展的 II 期临床试验(NCT07212933),首次探索脐带血来源 RAK 细胞治疗晚期胃癌的安全性与疗效。该研究采用随机对照设计,计划纳入 90 例一线治疗失败患者,通过剂量递增确定最大耐受剂量,重点评估总生存期(OS)与无进展生存期(PFS),预计 2028 年完成。
PAK免疫疗法与 CAR-T、NK 疗法的差异化竞争力
对比维度 | RAK 免疫疗法 | CAR-T 疗法 | CAR-NK 疗法 |
细胞来源 | 自体外周血 / 脐带血 | 自体 T 细胞 | 异体 NK 细胞 |
MHC 依赖性 | 非依赖 | 非依赖 | 非依赖 |
主要毒性 | 轻微疲劳 / 注射反应 | CRS、神经毒性 | 低毒性 |
实体瘤疗效 | 已验证(肝癌 / 肾癌) | 有限 | 探索中 |
制备周期 | 较短(体外扩增周期可控) | 较长 | 较短 |
适用场景 | 术后辅助 / 晚期治疗 | 血液瘤为主 | 广谱探索 |
RAK 疗法的核心优势在于:兼容自体 / 异体来源,安全性优于 CAR-T,实体瘤疗效数据更充分,且可通过剔除调节性 T 细胞进一步提升杀伤效率 —— 研究表明,清除抑制性 T 细胞后,RAK 细胞的增殖活性与肿瘤杀伤能力可提升 30% 以上。
从精准治疗到联合革命
1、适应症拓展:目前已在肺癌、结直肠癌、黑色素瘤等开展探索,未来有望覆盖更多实体瘤。
2、联合治疗策略:与 PD-1 抑制剂、化疗、介入治疗的协同效应正在验证,初步数据显示联合方案可使肿瘤退缩率提升至 50% 以上。
3、技术优化:通过基因编辑增强 RAK 细胞的肿瘤归巢能力,或结合肿瘤新抗原筛选实现 “个性化疫苗 + 细胞治疗” 的双重打击。
4、异体化突破:脐带血 RAK 的临床探索,有望解决自体细胞质量不佳(如晚期患者免疫功能低下)的痛点,实现 “现货型” 细胞疗法的普及。
RAK 免疫疗法以其温和的安全性、明确的实体瘤疗效,正在成为 CAR-T(血液瘤优势)与 NK 疗法(异体化优势)之外的 “第三极” 力量。从肝癌术后复发率的显著降低,到转移性肾癌的三线治疗突破,这项源于中国的创新技术,正通过持续的临床验证,为肿瘤患者开辟新的生存通道。随着联合治疗与异体化技术的成熟,RAK 疗法有望在免疫治疗的浪潮中,实现从 “小众选择” 到 “标准方案” 的跨越。

